Терагерцевое излучение повлияло на метаболизм клеток меланомы
- 03.04.2025
Биологи научно-исследовательского института клинической и экспериментальной лимфологии (НИИКЭЛ-филиал Института цитологии и генетики СО РАН, ИЦиГ СО РАН) совместно с коллегами из Новосибирского государственного университета (НГУ), ИЦиГ СО РАН и Института ядерной физики им. Г. И. Будкера (ИЯФ СО РАН) провели ряд экспериментов по исследованию воздействия терагерцевого излучения на клетки меланомы человека. Клетки облучались на Новосибирском лазере на свободных электронах (НЛСЭ) ИЯФ СО РАН с частотой излучения 2.3 ТГц и средней интенсивностью 0.05 Вт/см2 – генерация излучения с такими параметрами возможна только на этой установке. Метаболомный скрининг и биоинформатический анализ показали, что ТГц-излучение влияет на энергетический метаболизм клеток меланомы. Эти работы имеют фундаментальный характер и расширяют представление о биологических эффектах терагерцового излучения, а также клеточных реакций на его воздействие. Результаты опубликованы в журнале «Biochimica et Biophysica Acta (BBA) - Molecular and Cell Biology of Lipids».

Терагерцевое излучение (ТГцИ) находится между микроволновым и инфракрасным диапазонами электромагнитного спектра. Диапазон частот TГцИ составляет от 100 ГГц до 10 ТГц. Современные технологии, основанные на использовании электромагнитных волн терагерцевого диапазона, широко применяются в биомедицинских науках. Например, терагерцевая спектроскопия может быть актуальна в медицинской практике для диагностики онкологических заболеваний. В то же время ТГц-область изучена не полностью, поэтому фундаментальные исследования излучения данного электромагнитного спектра и в первую очередь изучение его биологических эффектов на живые системы являются актуальными.
«Наша работа посвящена изучению фундаментальных механизмов воздействия неионизирующего излучения на биологические объекты, в данном случае – на клетки меланомы человека. Однако целью исследования не является разработка методов лечения с использованием терагерцевого излучения, – прокомментировала младший научный сотрудник лаборатории клеточных технологий НИИКЭЛ-филиал ИЦиГ СО РАН Екатерина Бутикова. – В качестве модели мы выбрали клеточную линию меланомы, поскольку она является стабильной и хорошо изученной системой. Это позволяет минимизировать влияние побочных факторов и быть уверенными, что наблюдаемые изменения связаны именно с воздействием ТГц-излучения, а не с особенностями жизнедеятельности клеток».
Специалисты воздействовали ТГцИ на выращенные в культуральных флаконах клетки меланомы человека. Облучение на частоте излучения 2.3 ТГц проводилось на пользовательской станции Новосибирского лазера на свободных электронах.
«Новосибирский ЛСЭ является уникальным источником терагерцевого и инфракрасного излучения. По средней мощности он на много порядков превышает любые существующие в мире источники, что позволяет проводить абсолютно уникальные эксперименты в очень широкой области длин волн с различными биологическими объектами, – пояснил старший научный сотрудник ИЯФ СО РАН кандидат физико-математических наук Василий Попик. – Дело в том, что у биополимеров, таких как белки, существует четыре пространственных уровня организации. Если первичная структура определяется ковалентными связями, то вторичная, третичная и высшая определяются водородными связями, энергия которых лежит как раз в области ТГц-излучения. Поэтому если мы воздействуем ТГцИ на живые системы, то можем довольно сильно влиять на работу их клеток, на процессы, проходящие внутри них. Такие эксперименты представляют интерес с той точки зрения, что ни у одного живого организма не сформировано никаких защитных механизмов от ТГц-излучения, так как оно полностью поглощается атмосферой, а значит, воздействуя им на биологические объекты, можно исследовать, каким образом они приспособляются, какие механизмы защиты включают. Для подобных биологических экспериментов на НЛСЭ была создана специальная пользовательская станция, на которой реализована технология регулировки средней и пиковой мощности излучения, а также интенсивности воздействия. Так как мы работаем с живыми системами, которые комфортно себя чувствуют в очень узком температурном диапазоне, немаловажным для чистоты экспериментов было оборудовать станцию обтюратором и тепловизором – эти устройства поддерживают и контролируют нужную температуру. Благодаря этому мы понимаем, что получаем реакцию системы именно на воздействие облучения, а не на повышение или понижение температуры».
В эксперименте участвовали три группы клеток. Одну облучали терагерцевым излучением, вторую – инфракрасным излучением (ИК), третья была контрольная. Группы ТГц и ИК облучали по 10 и 45 минут. В день облучения специалисты проводили цитотоксические тесты клеток. На третьи сутки проводили метаболомный скрининг – анализ метаболитов, или органических молекул, участвующих в обмене веществ.

«Метаболиты – это малые органические молекулы, которые участвуют в обмене веществ в живых организмах. Они могут быть промежуточными или конечными продуктами биохимических реакций, обеспечивать клетки энергией, служить строительным материалом для клеток или выполнять регуляторные функции. В ходе сложных биохимических превращений одни вещества синтезируются, другие разрушаются, обеспечивая энергетический баланс, биосинтез и регуляцию клеточных функций, – добавил младший научный сотрудник Лаборатории физиологически активных веществ Новосибирского института органической химии им. Н.Н. Ворожцова СО РАН (НИОХ СО РАН), лаборант-исследователь Лаборатории молекулярной патологии Института медицины и медицинских технологий НГУ Никита Басов, – для исследования биохимического состояния клеток и тканей одним из наиболее эффективных инструментов является метаболомный скрининг. Он позволяет зафиксировать изменения в метаболическом составе организма, связанные с физиологическими процессами, заболеваниями или внешними воздействиями. Анализ широкого спектра метаболитов помогает заглянуть в молекулярный мир клетки и понять, как она функционирует. В нашей лаборатории мы проводим метаболомный скрининг методом высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрической детекцией (ВЭЖХ-МС/МС). Два года назад мы разработали подход, позволяющий анализировать около 400 метаболитов (включая как полярные соединения, так и липиды) менее чем за 30 минут анализа. Это стало возможным благодаря использованию монолитной колонки для ВЭЖХ, созданной сотрудниками Института катализа СО РАН Ю.С. Сотниковой и Ю.В. Патрушевым».
По словам Никиты Басова, ранее они применяли свой подход к метаболомному скринингу для анализа плазмы крови и сухих пятен крови, но его использование для исследования клеточных культур оставалось неизученным. «В рамках данной работы мы разработали и протестировали протокол пробоподготовки клеток, оценили его ограничения, а также впервые объединили его с аналитической методикой для изучения воздействия терагерцевого излучения на клетки меланомы», – пояснил он.
Благодаря данным метаболомного скрининга и использованию биоинформатических инструментов группа ученых пришла к выводу, что терагерцевое излучение влияет в первую очередь на энергетический метаболизм клетки. Для этого применялся инструмент ANDSystem – автоматизированная система, объединяющая данные из многочисленных биологических баз данных и научных публикаций, позволяя выявлять функциональные связи между генами, белками и метаболическими путями.
«Наши исследования показывают, что ТГц-излучение вызвало изменения в содержании 40 метаболитов, главным образом в путях пуринового и пиримидинового обмена, а также оно влияет на уровень церамидов и фосфатидилхолинов, – добавила Екатерина Бутикова. Анализ генетических сетей, проводившийся нашими коллегами из Лаборатории компьютерной протеомики ИЦиГ СО РАН, выявил митохондриальные мембранные белки как ключевые регуляторы биосинтеза этих метаболитов. Кроме того, ТГц-излучение, по-видимому, нарушает структуру липидных рафтов, что влияет на митохондриальный транспорт, но при этом не затрагивает целостность белков. Метаболические эффекты были специфичны для ТГцИ и отличались от теплового воздействия, наблюдаемого при инфракрасном излучении».
Фото 1: Культуральные флаконы с клетками меланомы в инкубаторе. Фото Е. Бутиковой.
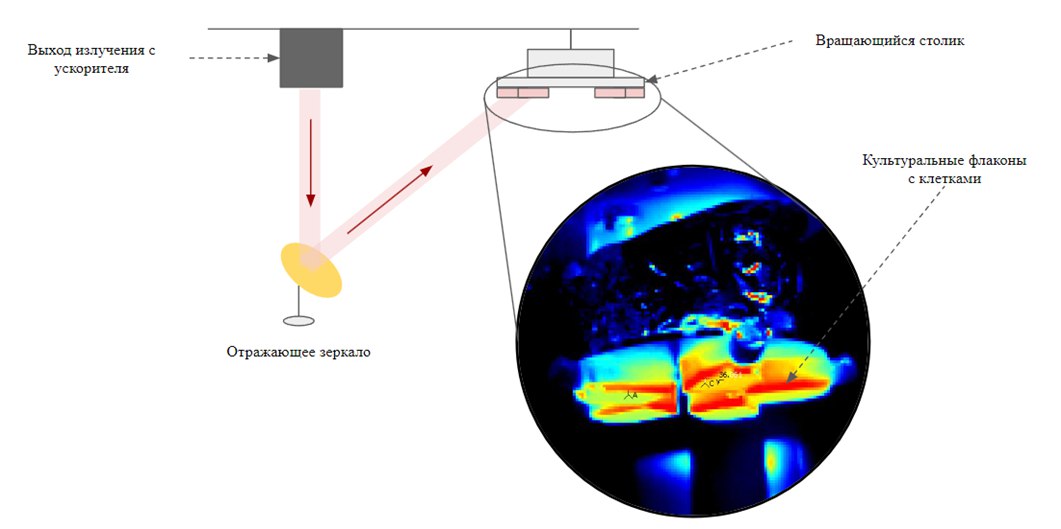
Фото 2:Схема пользовательской биологической станции на НЛСЭ. Позиционирование объекта исследования на станции. Предоставлено Е. Бутиковой.
Фото 3: Младший научный сотрудник лаборатории клеточных технологий НИИКЭЛ - филиал ИЦиГ СО РАН Екатерина Бутикова на пользовательской станции НЛСЭ во время эксперимента. Фото Н.Басова.
