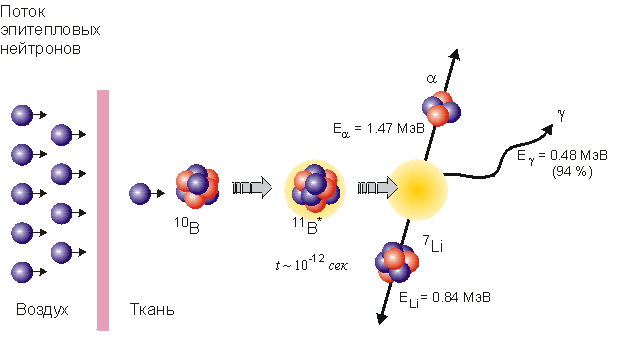
Образующиеся a -частица и ион 7Li быстро тормозятся и выделяют энергию 2,3 МэВ на длине порядка 10 микрон, т.е. на длине размера клетки. Такое быстрое торможение и, соответственно, громадный локальный нагрев приводит к поражению именно той клетки, которая содержала ядро бора. Т.о., если обеспечить более высокую концентрацию 10В в раковой клетке по сравнению со здоровой, то борнейтронзахватная терапия позволит осуществить избирательное поражение раковой опухоли.
Конечно, есть еще ряд ядер, которые имеют большое сечение захвата нейтрона, но ядро 10В предпочтительнее по следующим причинам. Во-первых, этот изотоп бора нерадиоактивен и легко доступен. Распространенность в природе изотопа с массовым числам 10 составляет примерно 20 %. Во-вторых, образующиеся в результате реакции энергетичные частицы быстро тормозятся и передают энергию. В-третьих, длина торможения порядка размера клетки. И, в-четвертых, хорошее понимание химии бора позволяет легко получить множество различных химических структур, содержащих бор.
При облучении ткани нейтронами помимо ядерных реакций, связанных с захватом нейтрона ядром бора, возможны и ядерные реакции 14N(n,p)14C и 1H(n,g )2H, которые приводят к появлению протонов отдачи и g -квантов. Хотя сечения захвата нейтрона водородом и азотом на несколько порядков меньше сечения захвата нейтрона изотопом 10В, но водород и азот присутствуют в такой большой концентрации, что это дополнительное неизбирательное "фоновое" облучение протонами отдачи и g -квантами вносит значительный вклад в поглощенную дозу. Для того, чтобы уменьшить влияние этого "фонового" облучения необходимо обеспечить достаточно высокую концентрацию бора в раковой опухоли.
В 1951 году Sweet с коллегами [2] впервые продемонстрировал, что определенное соединение с бором позволяет получить более высокую концентрацию бора в раковой опухоли по сравнению со здоровой клеткой. В течение 1950-60 гг. в Brookhaven National Laboratory [3, 4] и Massachusetts Institute of Technology [5] на специально построенных медицинских реакторах были проведенные первые клинические испытания, в которых применялись тепловые нейтроны и sodium borocaptate (Na210B12H11SH). К сожалению, эти клинические испытания не продемонстрировали терапевтическую эффективность данного метода. Причина заключалась в низкой концентрации бора, из-за чего "фоновое" облучение протонами отдачи и g -квантами в результате реакций 14N(n,p)14C и 1H(n,g )2H было достаточно велико.
Несмотря на неудачу, японский нейрохирург Хатанака, который участвовал в клинических испытаниях в США, вернувшись в Японию в 1968 году продолжил развитие этой методики. Он трепанировал череп, на открытом мозгу проводил хирургическую операцию, а затем облучал опухоль пучком медленных нейтронов с энергией ниже комнатной температуры. Такой методикой несколько групп в Японии на различных реакторах пролечили более 200 пациентов с очень обнадеживающими результатами [6, 7]
Параллельно большой прогресс был достигнут в синтезировании содержащих изотоп 10B фармпрепаратов. Получены препараты, которые создают концентрацию изотопа 10B в опухолевой ткани до 40 мкг/г, что в 3,5 раза больше, чем в здоровой ткани. Такая концентрация позволяет сделать вклад фонового облучения приемлемо малым и действительно обеспечить возможность избирательного поражения раковой опухоли.
Достижения Хатанаки и прогресс в синтезировании фармпрепаратов привели к тому, что в 1994 году возобновилось лечение пациентов с глиобластомой мозга на реакторах в Брукхевене и Массачусетсе. В 1997 году клинические испытания начались в Голландии, в 1999 году - в Финляндии. Сейчас к этим работам подключились в Англии, Австралии, Аргентине, Италии, Германии, Швеции, Чехии, России и др. странах. Очень обнадеживающие результаты получены также при терапии меланомы. В стадии изучения находится бор нейтронозахватная терапия рака полости рта, рака щитовидной железы и неонкологическое применение - лечение ревматического артрита.
Целесообразность развития технологии нейтронозахватной терапии обусловлена тем, что она ориентирована на лечение таких видов злокачественных опухолей, которые практически не поддаются никаким другим методам, - глиобластомы мозга и метастазы меланомы. Так, ежегодно примерно 1 человек из каждых 20000 поражается глиобластомой мозга. Исход всегда фатальный и обычно наступает через полгода. Хирургия или традиционная радиотерапия не останавливают распространение опухоли по всему мозгу и позволяют разве что продлить жизнь на год.
Прогресс бор-нейтронозахватной терапии в клинических испытаниях на реакторах и потенциальная востребованность методики привели к интенсивному обсуждению вопроса разработки и создания нейтронного источника на основе компактного и недорогого ускорителя, которым можно было бы оснастить практически каждую онкологическую клинику. Были предложены ускорительные системы, отвечающие основным требованиям нейтронозахватной терапии [8-13]: электростатические квадрупольные (ESQ), тандемные каскадные (TCA) и высокочастотные квадрупольные (RFQ). Недостатком ESQ систем, о чем свидетельствует многолетний опыт обслуживания, является расположение источника положительных ионов водорода под потенциалом 2,5 МВ. TCA системы обладают несомненным преимуществом в том, что ионный источник расположен под земляным потенциалом и требуется в два раза меньшее напряжение. Однако ионная оптика и конструкция ускорительной трубки, обеспечивающая требуемую скорость откачки и высоковольтную прочность, ограничивают прохождение стационарного пучка 1 или 2 мА. Наиболее привлекательным из ранее проверенных ускорителей является RFQ. RFQ система проста в работе, имеет невысокие эксплуатационные расходы и ионный источник располагается под земляным потенциалом. Однако она очень дорогостоящая, и наибольший ток, полученный к настоящему времени, составляет только несколько миллиампер.
Необходим был новый подход в ускорительной концепции для получения требуемого спектра и потока эпитепловых нейтронов в относительно компактной и недорогой системе. Новаторский подход в концепции нейтронного источника, предложенный нами в 1998 году [14], базируется на использовании электростатического тандемного ускорителя с вакуумной изоляцией VITA (vacuum insulation tandem accelerator) и припорогового режима генерации нейтронов [15, 16]. Стационарный пучок отрицательных ионов водорода инжектируется в электростатический ускоритель-тандем с вакуумной изоляцией и после перезарядки отрицательных ионов водорода в протоны в перезарядной мишени на выходе из тандема формируется протонный пучок, ускоренный до энергии, соответствующей удвоенному потенциалу высоковольтного электрода. При сбросе протонного пучка на литиевую мишень в результате пороговой реакции 7Li(p,n)7Be генерируется поток нейтронов. Наиболее привлекательный новаторский режим генерации нейтронов реализуется при энергии протонов 1,889-1,9 МэВ, что на 10-20 кэВ выше порога реакции. В этом случае кинематически коллимированный вперед в конусе с углом ~25° нейтронный пучок со средней энергией 30 кэВ может быть прямо использован для БНЗТ. Во втором режиме при энергии протонов 2,5 МэВ образующиеся нейтроны имеют более сложный и широкий спектр вплоть до энергии 790 кэВ и могут быть непосредственно использованы для терапии быстрыми нейтронами или для БНЗТ с помощью замедлителей, коллиматоров и отражателей. Отличительной особенностью всего проекта являются получение протонного пучка током в десятки миллиампер, обеспечивающего время экспозиции в десятки минут для достижения необходимой терапевтической дозы 20 Гр.
[1] G. Locher, Biological Effects and Therapeutic Possibilities of Neutrons, Am. J. Roentgenol. Radium Ther. 36 (1936) 1.
[2]. W. Sweet, M. Javid, The possible Use of Neutron-capturing Isotopes such as boron-10 in the treatment of neoplasms, I. Intracranial Tumors, J. Neurosurg., 9 (1952) 200-209.
[3] L. Farr et al. Neutron Capture Therapy with Boron in the Treatment of Glioblastoma Multiforme, Am. J. Roentgenol. 71 (1954) 279-291.
[4] J. Godwin et al. Pathological study of eight patients with glioblastoma multiforme treated with by neutron capture radiation using boron 10, Cancer (Phila.), 8 (1955) 601-615.
[5] Asbury et al. Neuropathologic Study of Fourteen Cases of Malignant Brain Tumor Treated by Boron-10 Slow Neutron Capture.Therapy, J. Neuropathol. Exp. Neurol. 31 (1972) 278-303.
[6] H. Hatanaka, Clinical results of boron neutron capture therapy. Basic Life Sci 54 (1990) 15-21.
[7] H. Hatanaka, Y. Nakagawa, Clinical results of long-surviving Brain Tumor Patients who underwenr boron neutron capture therapy. Int J Radiat Oncol Biol Phys 28 (1994) 1061-1066.
[8] Yanch et al. Medical Physics 19 (1992) 709.
[9] K. Wang, T. E. Blue, R. A. Gahbauer, Nucl. Technol. 84 (1989) 93.
[10] O. Anderson et al. Proc. 4th Europ. Particle Accelerator Conf., London, June 27 - July 21, 1994.
[11] Proc. 1st Int. Workshop on Accelerator-based Neutron Sources for BNCT. Jackson, Wyoning, USA. CONF-940976, 1994.
[12] Advances in Neutron Capture Therapy. v. 1, Medicine and Physics. Ed. By B.Larsson, Elseiver, 1997.
[13] Application of Accelerators in Research and Industry. Ed. By J. Duggan. AIP Conf. Proc. 392, NY, 1997.
[15] Кононов В. Н. и др. Доклады 2-го Всесоюзного совещания по применению ускорителей заряженных частиц в народном хозяйстве. Том 2, Л. НИИЭФА, 1976 г. стр. 60-68.
[16] V. Kononov et al. Proc. 1st Workshop on Accelerator-Based Neutron Sources for BNCT, Sept. 11-14, 1994, Jackson, USA, CONF-94096, v. 2, p. 447.
Используемые вещества Источник отрицательных ионов водорода Реакция рождения нейтронов Энергия протонов Это интересно
 ..
..